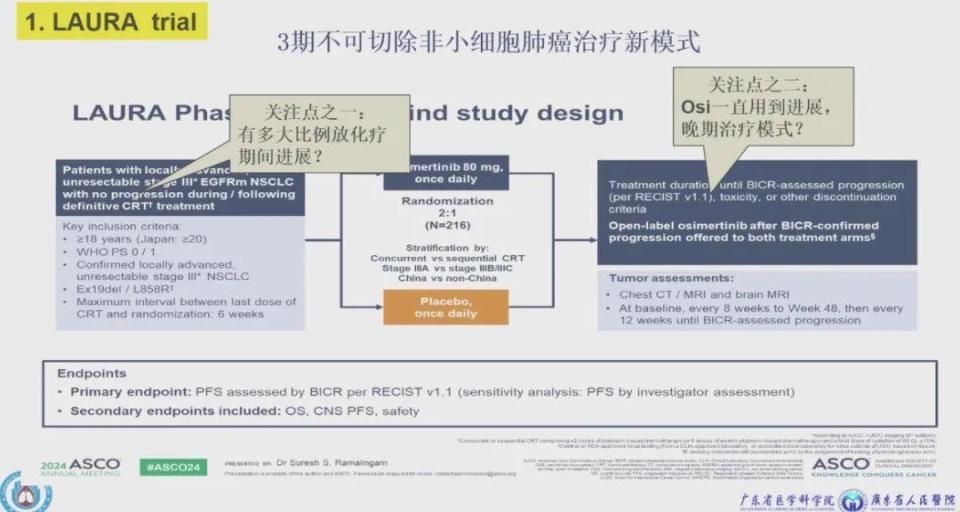
2024 年在 NEJM 上共发表了 6 篇肺癌领域的研究,其中 3 篇来自中国学者,而在 JAMA 和 Lancet 上共发表了 4 篇肺癌领域的研究,其中 2 篇出自中国学者;同时,今年中国药品监督管理局(NMPA)批准了十余项新型药物和疗法,部分药物的获批已走在美国食品药品监督局(FDA)之前。那么 2024 年最重磅的研究都有哪些?新型药物和新型疗法的获批又提示了怎样的发展方向?12 月 27 日,由广东省人民医院、广东省肺癌研究所吴一龙教授团队精心筹备的一年一度肺癌年终大盘点如期而至,在会议上,吴一龙教授为大家带来了「2024 肺癌大事件」的报告。丁香园肿瘤时间现将内容整理如下,以飨读者。LAURA 研究是全球首个评估奥希替尼作为 EGFR 突变 III 期不可切除 NSCLC 根治性放化疗后巩固靶向治疗的国际多中心、随机对照、双盲、III 期临床试验。结果显示,与安慰剂组相比,奥希替尼使 EGFR 突变 III 期不可切除 NSCLC 患者的中位无进展生存期(mPFS)显著延长 33.5 个月,疾病进展或死亡风险降低 84%。随后,欧洲肿瘤内科学会(ESMO)大会上进一步公布了其中枢神经系统(CNS)和远处进展结果,并发现奥希替尼在 CNS PFS(NR vs 14.9 个月,HR = 0.17)和至远处转移或死亡时间(TTDM,NR vs 13.0 个月,HR = 0.21)方面也展现出有临床意义的改善。这些突破性结果不仅填补了 EGFR 突变 NSCLC 精准治疗的最后一块空白,也标志着奥希替尼实现了在 EGFR 突变 NSCLC 各分期患者精准治疗的全覆盖。LAURA 研究数据发表后,立刻改变了临床实践,其重要性毋庸置疑,而吴一龙教授提出了两个值得关注的地方。根据研究设计,在同步放化疗期间出现疾病进展的患者将无法接受奥希替尼巩固治疗,那么这部分患者占比有多少?他们的治疗方式如何?
根据研究设计,患者持续用药直至疾病进展,治疗方案类似 IV 期患者。过去一直认为 III 期 NSCLC 是一种可以治愈的疾病,而从该研究的数据来看,这一观念似乎有所动摇。
 而随后报告结果的 POLESTAR 研究又在中国患者中验证了 LAURA 模式的可行性。 POLESTAR 研究是一项全中国多中心、随机、双盲、对照、III 期临床研究,评估阿美替尼在不可切除 EGFR 敏感突变患者放化疗后维持治疗的疗效与安全性。截止中期分析,阿美替尼组的 mPFS 为 30.4 个月,是安慰剂组 3.8 个月的 8 倍(HR=0.200)。ADRIATIC 研究是一项国际多中心、随机双盲的 III 期临床试验,旨在评估同步放化疗后未出现疾病进展的小细胞肺癌(SCLC)患者接受度伐利尤单抗联合或不联合曲美木单抗巩固治疗的疗效和安全性。研究采用了双主要终点设计:经独立评审委员会评估的 PFS 和总生存期(OS)。度伐利尤单抗组的 mOS 较安慰剂组延长了近两年(55.9 个月 vs. 33.4 个月),死亡风险降低了 27%(HR = 0.73,p = 0.01)。在 PFS 数据方面,度伐利尤单抗组的中位 PFS 较安慰剂组延长 7.4 个月(16.6 个月 vs 9.2 个月),疾病进展或死亡风险降低了 24%(HR = 0.76,p = 0.02)。吴一龙教授表示,ADRIATIC 研究实现了双终点阳性,建立了 LS-SCLC 放化疗后免疫巩固治疗的崭新治疗模式,也是 LS-SCLC 近 30 年来治疗方式的新突破。而该研究之后,SCLC 治疗领域留给大家最大的问题就是,外科在 SCLC 中的作用到底如何?这个话题仍待进一步的探索。2024 ASCO 年会和 J Clin Oncol 杂志于此前同步报道了 CROWN 研究的 5 年随访数据。结果显示,洛拉替尼一线治疗 ALK 阳性晚期 NSCLC 患者的 mPFS 突破 60 个月且仍未达到(HR = 0.19),5 年 PFS 率高达 60%。与克唑替尼相比,使用洛拉替尼治疗的患者疾病进展或死亡风险降低 81%。此外,洛拉替尼的中位缓解持续时间(DoR)仍未达到。在基线脑转移患者中,洛拉替尼组的中位颅内进展时间(IC TTP)仍未达到(95%CI:NR-NR),相较于克唑替尼组,其颅内进展风险降低了 94%(HR = 0.06)。同时,洛拉替尼组第 3 年、第 4 年、第 5 年的无颅内进展率均为 92%。在基线无脑转移患者中,洛拉替尼对于脑转移的预防效果同样优于克唑替尼,二者颅内进展时间的 HR 为 0.05(95%CI:0.02-0.13),且洛拉替尼组预防脑转移的 5 年无颅内进展率高达 96%(95%CI:89%-98%)。可见,在长期随访中,不论是否伴有脑转移,洛拉替尼都持续为患者带来了非常好的获益。吴一龙教授表示,CROWN 研究目前仍在随访之中,让我们一起期待它的 10 年随访结果,或许届时,NSCLC 将真正步入「慢病时代」,患者将实现「与癌共舞」。
而随后报告结果的 POLESTAR 研究又在中国患者中验证了 LAURA 模式的可行性。 POLESTAR 研究是一项全中国多中心、随机、双盲、对照、III 期临床研究,评估阿美替尼在不可切除 EGFR 敏感突变患者放化疗后维持治疗的疗效与安全性。截止中期分析,阿美替尼组的 mPFS 为 30.4 个月,是安慰剂组 3.8 个月的 8 倍(HR=0.200)。ADRIATIC 研究是一项国际多中心、随机双盲的 III 期临床试验,旨在评估同步放化疗后未出现疾病进展的小细胞肺癌(SCLC)患者接受度伐利尤单抗联合或不联合曲美木单抗巩固治疗的疗效和安全性。研究采用了双主要终点设计:经独立评审委员会评估的 PFS 和总生存期(OS)。度伐利尤单抗组的 mOS 较安慰剂组延长了近两年(55.9 个月 vs. 33.4 个月),死亡风险降低了 27%(HR = 0.73,p = 0.01)。在 PFS 数据方面,度伐利尤单抗组的中位 PFS 较安慰剂组延长 7.4 个月(16.6 个月 vs 9.2 个月),疾病进展或死亡风险降低了 24%(HR = 0.76,p = 0.02)。吴一龙教授表示,ADRIATIC 研究实现了双终点阳性,建立了 LS-SCLC 放化疗后免疫巩固治疗的崭新治疗模式,也是 LS-SCLC 近 30 年来治疗方式的新突破。而该研究之后,SCLC 治疗领域留给大家最大的问题就是,外科在 SCLC 中的作用到底如何?这个话题仍待进一步的探索。2024 ASCO 年会和 J Clin Oncol 杂志于此前同步报道了 CROWN 研究的 5 年随访数据。结果显示,洛拉替尼一线治疗 ALK 阳性晚期 NSCLC 患者的 mPFS 突破 60 个月且仍未达到(HR = 0.19),5 年 PFS 率高达 60%。与克唑替尼相比,使用洛拉替尼治疗的患者疾病进展或死亡风险降低 81%。此外,洛拉替尼的中位缓解持续时间(DoR)仍未达到。在基线脑转移患者中,洛拉替尼组的中位颅内进展时间(IC TTP)仍未达到(95%CI:NR-NR),相较于克唑替尼组,其颅内进展风险降低了 94%(HR = 0.06)。同时,洛拉替尼组第 3 年、第 4 年、第 5 年的无颅内进展率均为 92%。在基线无脑转移患者中,洛拉替尼对于脑转移的预防效果同样优于克唑替尼,二者颅内进展时间的 HR 为 0.05(95%CI:0.02-0.13),且洛拉替尼组预防脑转移的 5 年无颅内进展率高达 96%(95%CI:89%-98%)。可见,在长期随访中,不论是否伴有脑转移,洛拉替尼都持续为患者带来了非常好的获益。吴一龙教授表示,CROWN 研究目前仍在随访之中,让我们一起期待它的 10 年随访结果,或许届时,NSCLC 将真正步入「慢病时代」,患者将实现「与癌共舞」。
在 2024 年 9 月举办的世界肺癌大会(WCLC)中,由周彩存教授领衔的 HARMONi-2 研究结果正式公布。HARMONi-2 研究是针对 PD-L1 阳性 NSCLC 人群一线治疗的大型 III 期临床研究,头对头比较了依沃西单抗与帕博利珠单抗的疗效。结果显示,依沃西单抗组的 mPFS 达到了 11.1 个月,较帕博利珠单抗组的 5.8 个月几乎翻倍;两组客观缓解率(ORR)分别为 50.0% vs. 38.5%。其他终点指标如 OS 等目前尚未成熟,期待后续结果的公布。该研究较为有争议的一点在于,对于 PD-L1 TPS 1-49% 的人群,对照组并未采取标准治疗方案;同时 OS 数据尚不成熟,PFS 获益最终能否转化为 OS 获益尚无定论。但 HARMONi-2 研究结果的问世,无疑掀起了巨大的讨论,或许自 2018 年来免疫治疗的基础将被动摇,NSCLC 的治疗格局将重新进入「三国演义」的互相争霸局面,当然,这也意味着患者的生存预后可能得到进一步的改善。
而目前正在进行头对头比较研究的药物并不只有双抗,PD-1/L1 抑制剂联合其他药物、新型 PD-1/L1 抑制剂等都在这场「王位」角逐中全力以赴,而我们,将见证这场「战争」最后的赢家。LAURA 研究和 ADRIATIC 研究完善了 NSCLC 和 SCLC 的治疗链条,给这部分患者提供了治疗选择,是「填补空白」的研究;CROWN 研究的长期随访结果让后续难以再有研究能够与之匹敌,可当「Best」研究的称号;HARMONi-2 研究成功挑战了 PD-1/L1 抑制剂的地位,或将重置 NSCLC 的治疗格局,因此可被认为是「Better」研究。
2024 年 ESMO 亚洲大会上公布了 BEAMION LUNG-1 试验 Ib 期队列 1 的最新研究数据,评估 zongertinib(BI 1810631)在治疗携带 HER2 突变阳性晚期 NSCLC 经治患者中的疗效。经中心审查确认,zongertinib 展现出卓越疗效:ORR 为 71%,疾病控制率(DCR)高达 93%。初步生存数据表明,zongertinib 缓解持久:6 个月 PFS 率和 DoR 率分别为 69% 和 73%。在数据截至时,仍有 55% 的患者仍在接受治疗。Zongertinib 作为一种在研分子药物,尚未获得任何医疗监管机构批准,其疗效及安全性仍有待验证,而其所展现的结果,已足以对 HER2 ADC 发起挑战。
c-MET 扩增——EGFR 耐药治疗模式的精准治疗2024 年 8 月,由广东省人民医院吴一龙教授与韩国首尔大学医院 Tae Min Kim 教授合作的一项国际多中心的 II 期临床试验(INSIGHT 2 研究)发表在权威期刊 The Lancet Oncology 上,探索了一种新型联合治疗方案——特泊替尼联合奥希替尼治疗 EGFR 突变且出现 MET 扩增的 NSCLC 患者的疗效和安全性。在接受特泊替尼联合奥希替尼治疗的 EGFR 突变型 NSCLC 患者中,ORR 达到了 50.0%(95%CI:39.7%-60.3%),其中,50% 达到了部分缓解,13% 保持了至少 6 周的疾病稳定,23% 的患者疾病进展,中位 DoR 为 8.5 个月(95%CI:6.1-NE),66% 的患者在 6 个月内没有病情进展,48% 在 9 个月内没有病情进展。INSIGHT 2 研究的结果表明,特泊替尼联合奥希替尼在 EGFR 突变 NSCLC 患者中,对于 MET 扩增介导的奥希替尼耐药具有潜在的治疗优势。该联合疗法为临床提供了有价值的参考,并为未来的研究方向奠定了基础。而在 INSIGHT 2 研究之后,还有两项针对 EGFR 突变且 MET 扩增的确定性研究(SAFFRON 和 SACHI 研究)。除了被动等待耐药的发生,是否可以将针对 MET 扩增的治疗前移呢?由吴一龙教授牵头的 III 期 SANOVO 研究旨在从源头遏制 MET 扩增/过表达耐药,为患者带来更好的生存结局。让我们共同期待它的长期随访结果。
LUMINOSITY II 期研究旨在评估 Telisotuzumab vedotin 在 c-Met 蛋白过表达的非鳞状 EGFR 野生型 NSCLC 患者中的疗效和安全性。结果显示,Telisotuzumab vedotin 治疗的患者 ORR 为 35.4%。其中,c-Met 高表达患者的 ORR 为 46.2%,中度表达患者的 ORR 为 22.7%。治疗的 mDoR 为 6.9 个月,高表达组为 8.3 个月,中度表达组为 6.9 个月。mOS 为 17.4 个月,高表达组为 25.4 个月,中度表达组为 17.0 个月。mPFS 为 5.5 个月,高表达组为 5.5 个月,中度表达组为 5.4 个月。BR31 研究共有 1415 例患者接受了随机治疗,中位随访时间为 60 个月。其中 1219 例(86%)为 EGFR-/ALK-。试验中的患者在接受手术和化疗后,随机分配接受度伐单抗或安慰剂治疗。研究结果显示,无论 PD-L1 状态如何,度伐利尤单抗均未改善患者无病生存期(DFS)。结合多项类似研究的结果,总的来说,辅助免疫治疗的效果似乎不如新辅助或围手术期免疫治疗。2024 年 WCLC 上公布了一项基于 CheckMate 816 和 CheckMate 77T 研究数据的 IPT 分析(患者个体水平层面分析),将围术期纳武利尤单抗和新辅助纳武利尤单抗方案进行了对比。结果显示,与单纯新辅助纳武利尤单抗相比,围手术期纳武利尤单抗治疗可以进一步改善 EFS(HR = 0.61,95%CI:0.39-0.97)。但吴一龙教授表示,这两项研究的随访时间不一致可能导致结果的不稳定性,我们期待 CheckMate 816 研究最终随访数据公布后再来回答这个问题;另外,未来重点的方向应该是哪些患者需要辅助治疗。一项在接受标准治疗(≥3 月)失败的携带 KRAS G12C 突变的晚期 NSCLC 中国受试者中开展的开放标签、单臂 II 期注册临床研究,共纳入 116 名受试者,均给予氟泽雷塞 600 mg BID 单药治疗。中位随访 15.1 个月后,ORR 为 49.1%,DCR 为 90.5%,mDoR 尚未达到,12 个月 DoR 率为 53.7%。mPFS 9.7 个月,12 个月 PFS 率为 37.9%;mOS 尚未达到,12 个月 OS 率为 54.4%。亚组分析显示,各亚组在氟泽雷塞单药治疗中获益基本一致,包括预后较差的脑转移患者。II 期 D1553-102 研究纳入了来自中国 43 家医院的 KRAS G12C 突变 NSCLC 成人患者,旨在评价格索雷塞单药治疗 KRAS G12C 突变 NSCLC 患者的疗效和安全性。2024 年 WCLC 上公布的数据显示,中位随访 12.3 个月时,ORR 为 52.0%,DCR 为 88.6%,mPFS 为 9.1 个月(95%CI:5.6-10.3),mOS 为 14.1 个月(95%CI:11.5-17.3)。吴一龙教授表示,如果无法研发出可显著延长生存期的新药,或许后续针对 KRAS G12C 的研究应该更多地聚焦于联合治疗方案。瑞普替尼治疗 ROS1 阳性 NSCLC 患者的 TRIDENT 研究结果显示,TKI 初治患者的 ORR 为 79%,mPFS 为 35.7 个月,mDoR 为 34.1 个月。在既往接受过一种 TKI 且未接受过化疗的患者(n = 56)中,ORR 为 38%,mDoR 为 14.8 个月。在基线具有可测量脑转移病灶的患者中,7/8 名未接受 TKI 治疗的患者和 5/12 名接受过 TKI 治疗的患者观察到了颅内应答。2024 年 WCLC 上公布的洛拉替尼后线治疗局部晚期或转移性 ROS1 阳性 NSCLC 患者的 II 期研究结果显示,在后线治疗中,洛拉替尼组的 ORR 达到了 44.6%,mPFS 达到 17.9 个月,mOS 尚未达到。洛拉替尼的透脑性十分出色,脑转移控制率高。本研究中,基线脑转移患者(n = 37)ICR-ORR 达到 43.2%,21.6% 的患者实现了完全缓解。通过新辅助治疗,有 25% 左右的 III 期不可切除 NSCLC 患者可转化为可切除状态,且积极手术可带来预后获益。「III 期不可切除 NSCLC」的定义或许将出现变化,目前相关临床研究正在积极开展中。2024 年 3 月 2 日在广州举办的肺癌高峰论坛,吴一龙教授公布了中国首部肺癌适应性治疗专家共识。适应性治疗英文名称为 adaptive treatment ,即在标准治疗的基础上,根据生物标志物的变化随时调整治疗策略(升阶和降阶),在毒性可耐受的基础上获得更好的疗效,最终实现患者更好获益。适应性治疗的加加减减理念已经深入到早期肺癌、局部晚期肺癌、晚期肺癌的各领域,其中离不开生物标志物的检测(肿瘤组织基因图谱、血液 ctDNA 动态变化、MRD、PD-L1,肿瘤突变负荷等)。共识指出适应性治疗的标志物一定是经临床验证的,能稳定地、动态预测无复发或无进展,或预测疗效。目前循环肿瘤 DNA-微小残留病灶(ctDNA-MRD)是唯一被中国肺癌适应性治疗专家共识推荐的分子标志物,其已经展现出在肺癌全病程中各个场景下区分不同预后亚组的能力。CTONG1602 研究首次证实了在晚期 NSCLC 患者中,ctDNA 配合其它检测指导驱动基因阳性患者适应性地「降阶使用靶向药」,不仅能确保患者的生存获益,还能通过「药物假期(Drug Holiday:长期使用某种药物达到满意疗效后,可以停用一段时间,进入观察阶段)」减轻患者的治疗负担。在当前讲究联合、强化的「加法」模式的主流思维下,本研究有望为肺癌靶向治疗的个体化应用提出新的方向,对其他长期用药的肿瘤治疗模式的探索具有重要借鉴意义;该研究也为「适应性治疗」中「标准治疗基础上实施降阶治疗」模式提供了依据。目前已有一些 ADC 获批上市,主要针对 HER2 靶点,但正如前文所说,目前 HER2 ADC 正在接受小分子靶向药物的挑战;另外的 ADC 临床试验部分成功,部分失败,整体「喜忧参半」。
TROPION-Lung01 研究纳入既往经治的伴或不伴可靶向驱动基因突变的局部晚期/转移性 NSCLC 患者,评估 Dato-DXd 单药治疗对比多西他赛的疗效和安全性。在意向性治疗(ITT)人群中未观察到 OS 显著延长,但在 EGFR 突变患者中观察到了 OS 显著获益,这一点也被 TROPION-Lung01 和 05 研究的汇总分析证实,FDA 也基于此授予 Dato-DXd 用于 EGFR-TKIs 及含铂治疗进展后的 EGFR 突变晚期 NSCLC 成人患者的突破性疗法认定。
虽然 ADC 在 EGFR 突变患者中取得了一定的进展,但针对 EGFR 突变 NSCLC 患者的疗法非常多,且 ADC 具有自身独特的安全性问题,联合用药特别是联合化疗有一定难度;相比之下,在治疗选择较少、「门槛较低」的 SCLC 领域,ADC 似乎更有前景。因此 ADC 的布局和定位需要谨慎考虑。
双特异性抗体(Bispecific Antibody,BsAb)经细胞融合、重组 DNA、蛋白质工程等技术制成,可同时或先后结合两种抗原或同一抗原不同表位,是有别于单抗及单抗联合用药的「单药」,具有独特的治疗优势。我国在双抗药物的研发上走在世界前列,但临床试验的设计应当更加「国际化」,以进一步帮助国产双抗走出国门,走向世界。
III 期 HARMONi-A 研究的期中分析结果在 2024 年 ASCO 大会上重磅公布,并同步发表于 JAMA。基于此研究的优异结果,依沃西单抗已于同年 5 月被国家药品监督管理局批准上市,联合化疗用于 EGFR-TKI 治疗进展的 EGFR 突变的局部晚期或转移性非鳞 NSCLC 的治疗。从长期疗效来看,其 OS 曲线在早期即出现分离,提示了明显的获益趋势。至数据成熟度达到 52% 时,试验组和对照组的 mOS 分别为 17.1 个月 vs 14.5 个月,依沃西单抗联合化疗可降低 20% 的死亡风险。期待后续随访中能够得到显著获益的结果。
BNT327/PM8002 是一种双特异性抗体候选药物,在一项 2 期临床试验(NCT05756972)中,BNT327/PM8002 与化疗联合使用,针对具有 EGFR 突变的晚期 NSCLC 患者,展现出令人鼓舞的抗肿瘤活性,无论患者的 PD-L1 状态如何,且安全性良好。
关于双抗的未来,吴一龙教授认为,双抗的第二波研究高潮正在出现,抗体组成更加多元化,双抗具有无限的发展空间,可能重塑癌症的治疗格局。