▎药明康德内容团队编辑
在细菌中,有一些被称作质粒的DNA结构游离于染色体之外,它们能够携带遗传信息也可以自主复制,为细菌提供一些性状支持。除了细菌,近些年的一些研究发现癌细胞也具备类似的特殊DNA,被称作染色体外DNA(ecDNA),通常以环状的形式游离在细胞核内部或外部,它们并不遵守常规的染色体分离机制。
更加值得关注的是,这种奇怪的DNA分子似乎对癌细胞的生存格外有利,例如胶质母细胞瘤的EGFR基因过度活跃,这些基因就倾向于形成环状ecDNA,来增加EGFR的水平。但目前,科学界对ecDNA的研究仍然不多,它们在癌细胞中的普及性有多少?如何在癌细胞子代间传递?人类能否通过靶向ecDNA来清除癌细胞?
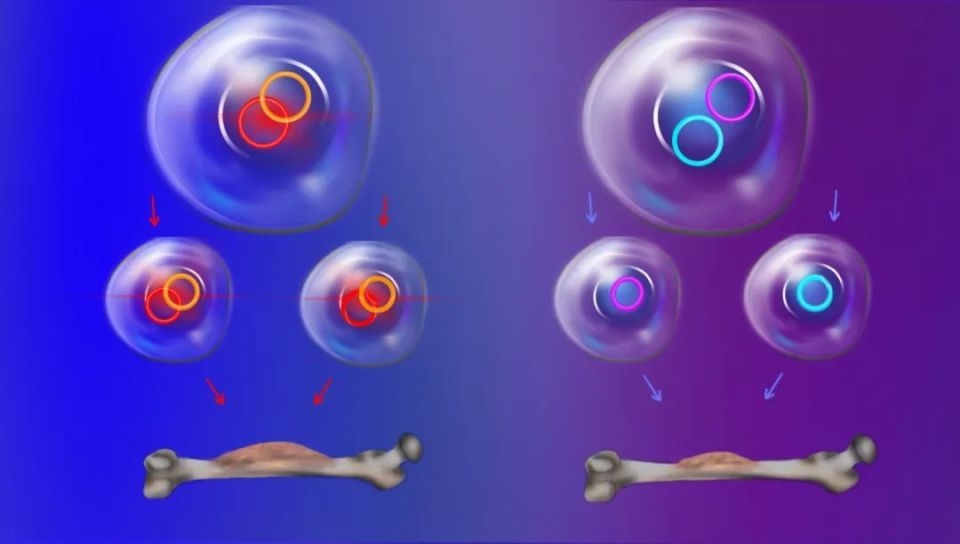
▲不同的环状ecDNA可能会联结并一起传递给子代细胞,这种模式可以显著推动肿瘤进展(左);完全随机分配模式则可能让优势性状分散(右)(图片来源:EMILY MOSKAL/STANFORD MEDICINE)
在今日的《自然》杂志上,来自斯坦福大学、弗朗西斯·克里克研究所、伦敦大学学院癌症研究所等多个研究单位发表了3篇研究论文,从多个角度刷新了我们对ecDNA的认知。来自斯坦福大学的Paul Mischel教授是三项研究的共同通讯作者,他指出,“每项研究都是突破性的,它们共同代表了认识癌症起源与演化的一个关键节点进展,也让我们了解了驱动癌症进展的一个常见机制。”
早在2017年,Mischel教授就曾在《自然》上发表论文,揭示了ecDNA的部分特征,比如正常细胞没有发现ecDNA的存在,而分析的癌症类型中接近一半都有ecDNA的踪迹。过往研究普遍认为大约2%的肿瘤中会出现ecDNA。在此次的一篇《自然》论文中,Mischel教授和同事共同对超过1.5万个肿瘤样本进行了全基因组测序,涉及到39种肿瘤类型。总体来看,ecDNA的出现频率远比过去推测的高,作者在17.1%的肿瘤样本中都检测到了ecDNA。此外,它的出现频率会因肿瘤类型而异,其中脂肪肉瘤有超过一半的样本存在ecDNA,另外胶质母细胞瘤、HER2+乳腺癌的ecDNA出现频率也接近50%。这些肿瘤中的ecDNA对癌细胞的演化非常重要,除了过往发现的癌基因扩增现象,新研究还发现有些ecDNA扩增了免疫调节相关基因,主要是用于下调免疫效应过程,或者淋巴细胞介导的细胞毒性,这些ecDNA可以减少T细胞浸润和杀伤性,帮助癌细胞实现免疫逃逸。研究还意外发现,有一些ecDNA本身并不包含编码基因,而是一些增强子DNA序列,它们自身没有明显功能,但是可以显著增强其他ecDNA的作用。数据显示,随着癌症患者接受化疗或者靶向疗法,ecDNA的出现频率会更高,这也代表着它们会随着癌细胞一同演化和发展。在中学课本上,我们学习过染色体的分离机制,分裂细胞两极的纺锤体可以通过牵引染色体使它们平均分配到子代细胞中。但是游离的ecDNA并不具备着丝粒,理论上来说它们会随机分配进入子代细胞。这种随机性可能会造成有的癌细胞ecDNA很多,有的则可能几乎没有ecDNA,这在一定程度上保证了一些癌细胞具备超强的能力,可以抵抗免疫系统和药物攻击。但这种随机分配也有一些问题,它会让有利的ecDNA组合太过于分散,而不能集中在某一子代细胞中,比如某一癌基因和增强子元件可能会分配到两个细胞中。癌细胞要如何保证将生存优势集中到一起呢?Mischel教授与斯坦福大学医学院的Howard Y. Chang教授团队共同解开了其中的谜团。他们发现细胞内的ecDNA可以分为特定的“种群”(species),能够互相协助获得更强功能的ecDNA会聚集到一起,在细胞分裂期间共同进行联结分离,并且这种分离过程不对称,往往是ecDNA种群一同传递到某一特定细胞内。▲一些ecDNA会联结传递到子代细胞中(图片来源:参考资料[2])更关键的是,为了保证同一种群的各个ecDNA水平一致,在有丝分裂过程中ecDNA会主动促进转录过程,这一点与染色体是完全不同的。当ecDNA转录过程没有全部完成时,还会抑制基因复制和有丝分裂,如此可以保证ecDNA种群能够作为一个整体分离到子代细胞中。这种机制让具有优势的性状总是能传递下去,这也是癌细胞的生存和发展之道。新研究与过往研究的一些数据都表明ecDNA在促进癌症发展,推动抗癌疗法耐药性方面有重要影响,这也让其有望成为一种全新的抗癌方向。我们刚刚提到,ecDNA的转录会暂时抑制基因组复制的进程,而在另一篇《自然》论文中,Mischel教授与Chang教授就从中看到了介入的可能性。他们的目标是增强癌细胞中这种转录与复制的冲突性。研究分析了ecDNA转录时活跃的介质,其中一个名为pRPA2-S33的分子会随着转录在ecDNA增加。同时,由于DNA复制被抑制,DNA上的复制叉处于停滞状态,这会引起级联信号并激活S期检查点蛋白CHK1,防止DNA复制完成之前就执行有丝分裂。作者尝试在含有ecDNA的肿瘤细胞中抑制了CHK1的活性,结果他们看到这些肿瘤细胞相继出现死亡。由于ecDNA转录没有停止,而又松开了基因复制上的限制因素,这导致转录与复制冲突性变强,加速了细胞死亡。从细胞实验和小鼠实验来看,CHK1抑制剂都能有效地阻止癌细胞的生长,并且接受治疗的肿瘤小鼠肿瘤体积消退明显,生存期更长。目前,CHK1抑制剂处于早期临床试验阶段,研究团队正计划进一步推动相关研究,帮助治疗那些ecDNA致癌特征明显的肿瘤类型。[1] Origins and impact of extrachromosomal DNA. Nature (2024). DOI: https://doi.org/10.1038/s41586-024-08107-3[2] Coordinated inheritance of extrachromosomal DNAs in cancer cells. Nature (2024). DOI: https://doi.org/10.1038/s41586-024-07861-8[3] Enhancing transcription–replication conflict targets ecDNA-positive cancers. Nature (2024). DOI: https://doi.org/10.1038/s41586-024-07802-5本文来自药明康德内容微信团队,欢迎转发到朋友圈,谢绝转载到其他平台。如有开设白名单需求,请在“学术经纬”公众号主页回复“转载”获取转载须知。其他合作需求,请联系wuxi_media@wuxiapptec.com。
免责声明:药明康德内容团队专注介绍全球生物医药健康研究进展。本文仅作信息交流之目的,文中观点不代表药明康德立场,亦不代表药明康德支持或反对文中观点。本文也不是治疗方案推荐。如需获得治疗方案指导,请前往正规医院就诊。