
结直肠癌是最常见的恶性肿瘤之一,全球发病率居恶性肿瘤第 3 位,死亡率居第 2 位。近年来,随着精准医学及靶向药物的发展,分子靶向药物已成为结直肠癌个体化治疗和综合治疗的一线方案,为结直肠癌患者带来更好的生存获益。相关分子标志物的检测对个体化方案的判定、预后判断及疗效预测等方面均起到重要作用。
目前国内外已有的相关指南及实践推荐检测的结直肠癌相关基因包括 RAS、BRAF 和 MMR 等。KRAS、NRAS 均参与表皮生长因子受体(EGFR)的信号转导,调控细胞生长、分化、增殖和存活。其中 KRAS 点突变的发生率为 40%~50%,NRAS 点突变为 3.8%。常规需要检测的位点包括 KRAS 和 NRAS 基因的第 2、3、4 号外显子。多项研究表明,RAS 野生型的晚期结直肠癌患者能从抗 EGFR 单抗治疗中获益,尤其对于原发灶位于左半结肠和直肠的患者;而对于 RAS 基因突变患者,无法从抗 EGFR 单抗中获益,一般采用化疗联合血管内皮生长因子(VEGF)单抗治疗。BRAF 基因位于 RAS 基因下游,是 RAS-RAF-MEK 激酶通路上的关键成员。BRAF 在亚洲结直肠癌患者中突变率为 5.4%~6.7%,其中 90% 为 BRAF V600E 突变,而非 V600E 突变结直肠癌整体预后与 BRAF 野生型相似,也不影响抗 EGFR 单抗的选择,因此 BRAF 非 V600E 突变检测尚不常规开展。NCCN 指南和 CSCO 指南对 BRAF V600E 突变转移性结直肠癌(mCRC)患者的二线治疗均推荐西妥昔单抗+伊立替康+维莫非尼(BRAF 抑制剂)或西妥昔单抗+BRAF 抑制剂 ±MEK 抑制剂的联合方案。微卫星不稳定(MSI)状态/错配修复
(MMR)蛋白表达
MSI 状态和 MMR 蛋白表达是包括结直肠癌在内的泛瘤种免疫检查点抑制剂效果的预测指标,其中 MSI-H/dMMR 整体发生率约 15%,在晚期结直肠癌中约占 5%。通常检测 5 个微卫星位点:BAT-25、BAT-26、D2S123、D5S346 和 D17S250;当 ≥2 个微卫星位点显示 MSI,即可诊断为 MSI-H;1 个显示 MSI,可诊断为 MSI-L;没有任何位点显示 MSI,即 MSS。而 MMR 相关蛋白为 4 个:MLH1、MSH2、MSH6 和 PMS2,其中 ≥1 种表达缺失,判定为错配修复基因缺陷(dMMR);全部阳性,则判定为错配修复基因完整(pMMR)。一般而言,dMMR 相当于 MSI-H,pMMR 相当于 MSI-L 或 MSS。MSI-H 状态的 Ⅱ 期和 Ⅲ 期结直肠癌患者,其预后一般优于 MSS 患者。MSI-H 的 Ⅱ 期患者,一般预后较好,且不能从氟尿嘧啶类单药化疗中获益,建议 Ⅱ 期患者术后常规进行 MSI 检测。
除上述常用分子标志物外,目前其他潜在的分子标志物在结直肠癌中的发生率低,临床意义及靶向治疗的反应性尚在评价中,如 Her-2 扩增/过表达、PIK3CA 突变、NTRK 融合和肿瘤突变负荷(TMB)等。结直肠癌中 Her-2 扩增/过表达的总体发生率约为 5%,与 KRAS、NRAS 和 BRAF 突变存在相互排斥,且在原发肿瘤与转移瘤之间高度一致。推荐对于经标准治疗失败后的 mCRC 患者可进行 Her-2 扩增/过表达的检测。目前 NCCN 指南和 CSCO 指南均推荐 Her-2 扩增/过表达患者可接受抗 Her-2 靶向药物的治疗(曲妥珠单抗联合帕妥珠单抗、曲妥珠单抗联合拉帕替尼),但两个指南的差别在于 CSCO 指南推荐在姑息三线及三线治疗以后使用,而 NCCN 指南则对姑息一线、不能耐受高强度治疗的患者也有抗 Her-2 治疗的推荐。NTRK 基因融合在结直肠癌中比较罕见,发生率为 0.35%。由于 NTRK 基因融合发生率极低,目前仅推荐在标准治疗失败后或者筛选临床研究的患者中进行检测。NTRK 抑制剂(拉罗替尼、恩曲替尼)仅对携带 NTRK 融合的患者有效,而对突变患者无效。PIK3CA 在中国人群中突变率仅为 3.5%,可与 RAS 突变共同存在。有研究表明 PIK3CA 突变可能是对阿司匹林治疗有效的预测标志物。此外,由于 PIK3CA 突变与抗 EGFR 单抗疗效的相关性目前尚不能完全确定,因此目前尚不推荐常规行 PIK3CA 突变检测。TMB 是肿瘤组织 DNA 中基因组突变数的指数,是测量肿瘤体细胞内编码蛋白的平均 1Mb 范围内的碱基突变数量,包括基因编码错误、碱基替换、基因插入或缺失等各种形式的突变。FDA 于 2020 年 6 月批准了免疫检查点抑制剂用于治疗高肿瘤突变负荷(TMB-H≥10 个突变/兆碱基)的无法切除或转移性实体瘤的成年和儿童患者。目前在结直肠癌中尚不推荐常规行 TMB 检测。《CSCO 结直肠癌诊疗指南(2024 版)》中强调了 POLE/POLD1 基因突变检测的重要性。POLE/POLD1 基因是 DNA 合成和损伤应答相关基因,部分发生在 POLE/POLD1 蛋白 DNA 外切酶结构域的突变会导致肿瘤超突变,这种功能性突变使肿瘤中免疫原性突变数量和质量提高,T 细胞被激活,功能增强,改善肿瘤免疫微环境,因此具有 POLE/POLD1 基因突变的患者对免疫治疗更加敏感且预后较好。2%~8% 的 MSS/pMMR 型结直肠癌具有体细胞的 POLE 功能性突变,而 POLD1 突变极其罕见,可以用单基因测序的方法进行检测,但大 panel 的 NGS 检测不仅可以检测到包括 POLE/POLD1 在内的基因改变,也可以获得 TMB 等数据。
结直肠癌相关蛋白表达的检测对判定肿瘤来源、类型、恶性程度、耐药和预后均有指导意义,常用于结直肠癌的鉴别诊断或辅助诊断。表 1. 与结直肠癌鉴别诊断/辅助诊断有关的免疫组织化学(IHC)标志物
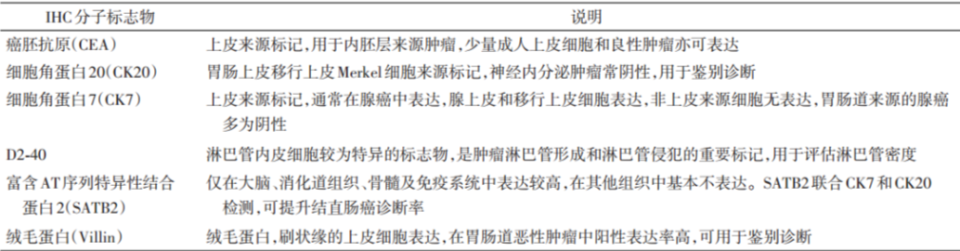
与结直肠癌相关的家族遗传性疾病:家族性息肉病、林奇综合征和黑斑息肉综合征(P-J 综合征)等;其中遗传易感基因包括 TP53、RB1、APC、MMR 和 STK-11 等。如 APC 突变与家族性腺瘤性息肉病(FAP)有关,如怀疑 FAP 而 APC 基因无突变者,还需要进一步检测 MUTYH 基因突变;林奇综合症发病与 MMR 基因的胚系突变有关,约 70% 由 MSH2 和 MLH1 突变所致,其余 30% 多由 MSH6 和 PMS2 突变所致。对结直肠癌的遗传易感性基因的检测需要在胚系细胞(精子、卵子)中检测才能明确,临床上常用外周血淋巴细胞或口腔黏膜细胞代替。在结直肠肿瘤中发现的突变如果在外周血淋巴细胞或口腔黏膜细胞中得到证实,就可推定患者所有细胞都携带有该突变,可以认为是胚系突变。综上所述,对于所有 mCRC 患者,均推荐在综合治疗前行常规分子标志物检测(RAS 基因突变、BRAF 基因突变、MSI 状态/MMR 蛋白表达),根据结果制定个体化治疗方案。对于经标准治疗失败的 mCRC 患者,可进行 Her-2 扩增/过表达、NTRK 基因融合以及 POLE/POLD1 基因突变的检测;PIK3CA 突变检测和 TMB 检测目前多用于临床研究。对于怀疑诊断家族性息肉病、林奇综合征和 P-J 综合征等家族遗传性疾病者,推荐行相关遗传易感性基因的胚系突变检测。基于上述分子标志物的检测,目前临床上针对结直肠癌靶向治疗主要包括抗 VEGF/VEGFR 为靶点、针对以 EGFR 为靶点的靶向治疗及多靶点激酶抑制剂类药物,具体如下:随着对结直肠癌发病机制的深入研究以及治疗新靶点的发现,相信靶向治疗药物会在未来结直肠癌的综合治疗中扮演更为重要的角色。[1] 中国临床肿瘤学会(CSCO)结直肠癌专家委员会. 结直肠癌分子标志物临床检测中国专家共识 [J] . 中华胃肠外科杂志, 2021, 24(3) : 191-197.[2] 中国医师协会结直肠肿瘤专业委员会, 中国抗癌协会大肠癌专业委员会, 国家癌症中心国家肿瘤质控中心结直肠癌质控专家委员会. 结直肠癌靶向治疗中国专家共识 [J/CD]. 中华普通外科学文献(电子版), 2023, 17(1) : 1-8.[3] 中国临床肿瘤学会(CSCO)结直肠癌诊疗指南(2024 版).