2024 年欧洲肿瘤内科学会(ESMO)年会以 LBA 的形式对 NATALEE 研究 4 年随访结果进行了口头报告,并且在报告后获得了在场专家的鼓掌致意。其结果显示在完成了瑞波西利 3 年辅助治疗后患者可持续获益,并且获益在延长随访时间后持续扩大,显示了其在包括 II 期,N0 有复发风险因素患者中的良好疗效。
基于 NATALEE 研究结果,目前美国食品药品监督管理局(FDA)已批准瑞波西利联合芳香酶抑制剂(AI),作为高复发风险的激素受体阳性/人表皮生长因子受体2阴性(HR+/HER2-)II 期和 III 期早期乳腺癌(EBC)患者的辅助治疗,包括无淋巴结转移(N0)的患者,获批范畴较以往 CDK4/6 抑制剂早期乳腺癌适用人群增加一倍有余。丁香园特邀复旦大学附属肿瘤医院邵志敏教授深入解读 NATALEE 研究的匠心设计和这次 4 年随访结果更新的重要意义。
NATALEE 研究匠心设计,纳入了更多当前内分泌单药治疗欠佳的 HR+/HER2− eBC 患者
乳腺癌是女性最常见的恶性肿瘤,超过 90% 患者在诊断时处于疾病早期阶段,即 I-III 期[1]。HR+/HER2- 是乳腺癌中占比最高的亚型,高达 70%[1]。在 CDK4/6 抑制剂获批前,辅助内分泌单药治疗是这类患者的标准术后治疗方案[1]。遗憾的是,尽管接受了标准内分泌治疗,仍有部分 HR+/HER2- 早期乳腺癌患者会复发转移,进展为不可治愈的疾病。因此在传统内分泌治疗基础上联合 CDK4/6 抑制剂辅助强化治疗是当前领域的重要探索方向。然而,既往 CDK4/6 抑制剂联合内分泌辅助治疗的 III 期临床试验显示出不同结果。阿贝西利的 monarch E 研究[2]取得了阳性成果,但该研究仅纳入了淋巴结阳性患者(其中 N1 需要伴有其他高风险临床特征)。因此,该研究入组人群仅占真实世界中 HR+/HER2− 早期乳腺癌患者的一小部分[3]。NATALEE 研究为一项全球多中心、随机对照、Ⅲ期临床试验,共纳入 5101 例 II-III 期 HR+/HER2-早期乳腺癌患者,1:1 分为瑞波西利+内分泌治疗或单独内分泌治疗组(图 1)。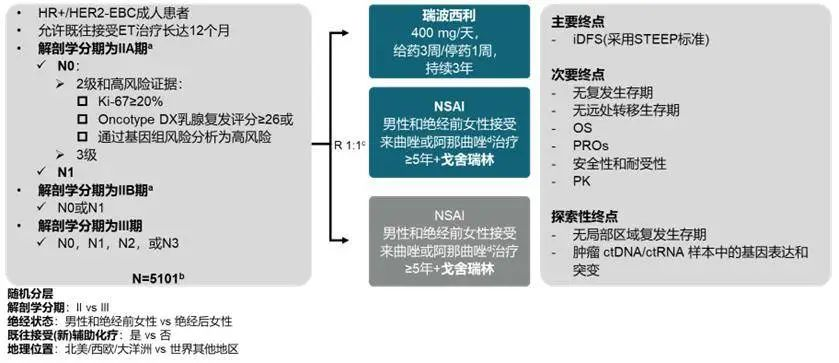
图1 NATALEE 研究设计
NATALEE 研究人群几乎包含了所有 IIA 到 IIIC 期 HR+乳腺癌患者,仅针对 T2N0 人群,必须满足 G3 或 G2(伴有 Ki-67≥20% 或基因组高风险)。从纳入人群特点上看,NATALEE 研究包括了 monarch E 研究中的所有入组人群,并且 II 期患者占比相对较多,纳入了 N0 伴复发风险和所有 II-III 期 HR+早期乳腺癌中的 N1 患者,更加贴合临床实际中具有复发风险人群的分布[4],旨在满足更多患者的未尽之需。既往 NATALEE 研究结果显示[5],与对照组相比,瑞波西利+内分泌治疗组针对意向治疗(ITT)人群的 iDFS 获益显著更优,3 年 iDFS 率的绝对获益率为 3.3%(90.4% vs 87.1%,P=0.003)。并且所有亚组患者(包括 N0、II 期、Ⅲ期等)中均观察到一致的获益趋势[6]。其中 N0 亚组结果在 2024 年美国临床肿瘤学会(ASCO)大会予以公布[7],瑞波西利+内分泌治疗组的 3 年 iDFS 率(93.2 vs 90.6%,HR = 0.723)、3 年 DDFS 率(94.3% vs 91.5%,HR = 0.703)、3 年 DRFS 率(96.3% vs 92.5%,HR = 0.580)均得到显著改善。基于 NATALEE 研究结果 FDA 已批准瑞波西利联合 AI,作为高复发风险的 HR+/HER2- II 期和 III 期 EBC 患者的辅助治疗,包括 N0 的患者,获批范畴较以往 CDK4/6 抑制剂早期乳腺癌适用人群增加一倍有余。
四年随访数据,进一步夯实瑞波西利在更广阔人群中确定的疗效,助力更多患者走向治愈
2024 年 ESMO 年会以 LBA 的形式对 NATALEE 研究 4 年随访结果进行了口头报告。本次报告所有患者中位随访时间为 44.2 个月,所有患者均已停止瑞波西利用药。其中 62.8% 的患者完成了瑞波西利全部三年治疗。该延长随访结果显示,与对照组相比,瑞波西利+内分泌治疗组针对意向治疗(ITT)人群的 iDFS 获益取得了进一步的扩大。4 年 iDFS 率的绝对获益率为 4.9%(88.5% vs 83.6%,P<0.0001)(图1)。并且所有亚组患者(包括 N0、II 期、Ⅲ期等)中均观察到一致的获益趋势[8]。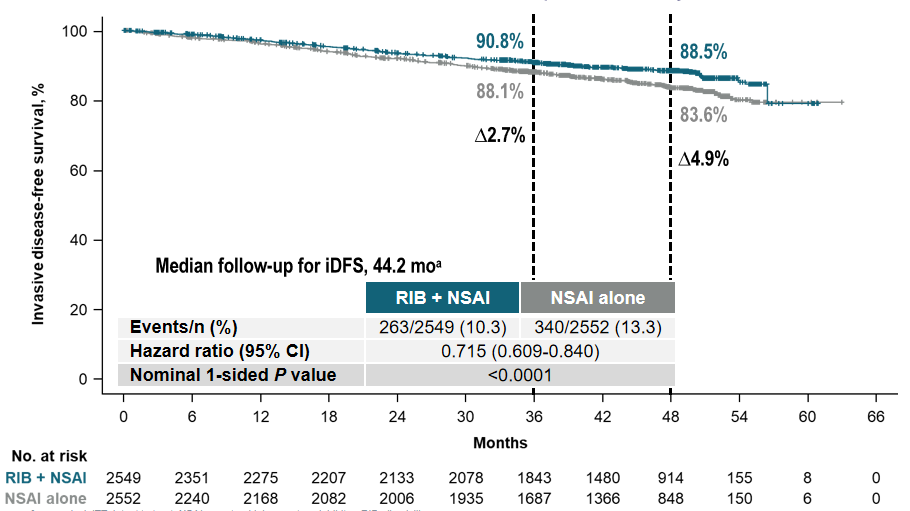
图1 NATALEE 研究中患者 4 年 iDFS 获益明显
尤其值得强调的是,本次公布的数据显示,在 NATALEE 纳入的 II 期亚组患者中,4 年 iDFS 的绝对值获益取得了 4.3% 的提高。N0 携带风险因素患者则取得了 5.1% 的提高。II 期及 N0 携带风险因素患者既往认为复发风险较低,但通过 NATALEE 研究的对照组可看出,这些患者在接受 AI 单药治疗 4 年时约有 10~13% 的患者会出现 iDFS 事件,复发风险不容小觑。本次 4 年 iDFS 数据再次证明了瑞波西利在这一人群中的确切疗效,并且打消了部分医生之前认为这一人群获益不够明显的疑虑(图2)。考虑到这部分患者复发常常较晚,可能随着随访时间延长,瑞波西利组带来的疗效改善会更加显著。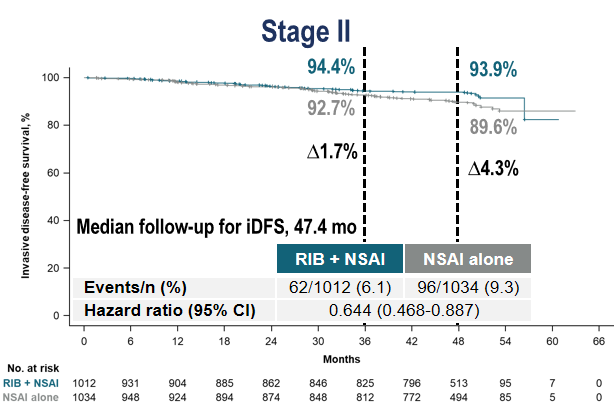
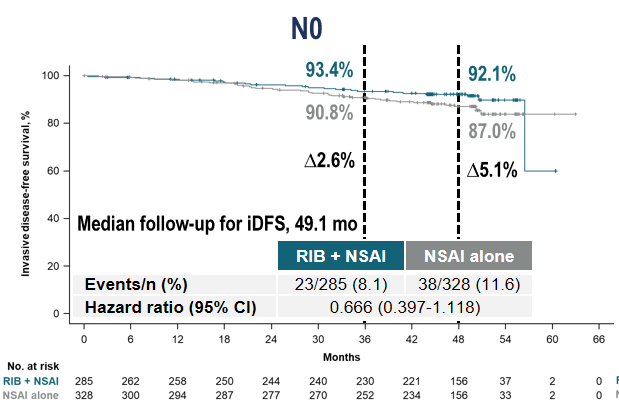
图2 II 期人群和 N0 人群获益明显
在与 monarchE 研究重叠度较高的 III 期人群中,NATALEE 研究取得了 5.9% 的 iDFS 提升。这一数据也证明了瑞波西利所带来的获益可在 NATALEE 全人群中得到展现。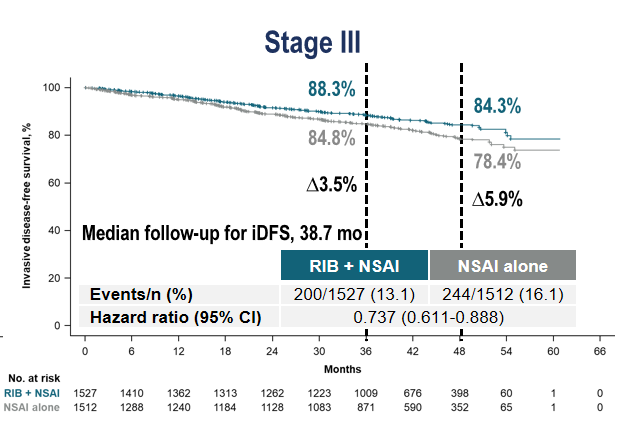
图3 III 期人群获益显著
安全性方面,相较于上次数据汇报时变化不大,在中位随访延长 11 个月后,因为 AE 停止治疗的人数只增加了 0.5%。这里需要明确的是,根据研究方案要求,如果患者在瑞波西利治疗期间肝酶不能在 28 天恢复正常则必须进行停药,而 monarchE 研究中没有类似的要求。所以非常期待瑞波西利在真实世界中对肝脏功能的影响及其对治疗的意义。本次大会还同步报告了 NATALEE 研究的 OS 结果,在中位随访 44.3 个月时,瑞波西利组相对于内分泌单药组取得了 HR 0.827 (0.636-1.074,P =0.08)的结果。这一 OS 结果相对于中位随访 35.9 个月时的 HR 0.892 又取得了一些进展,期待在更长随访时间后,瑞波西利可以续写晚期 OS 奇迹,再次在早期乳腺癌研究中取得有统计学差异的 OS 结果。总之,NATALEE 是目前 CDK4/6 抑制剂辅助治疗 III 期研究中纳入最广泛 HR+/HER2-早期乳腺癌患者的临床研究,其获益人群拓展至几乎所有 II-III 期,包括 N0 伴有复发风险以及全部 N1 患者,更加符合临床实际中具有复发风险的早期乳腺癌患者分布。本次 4 年随访数据的公布再次验证了瑞波西利对这一更广阔人群的疗效,显著提高了这类人群实现治愈的机会。基于 NATALEE 研究结果 FDA 已批准瑞波西利联合 AI,作为高复发风险的 HR+/HER2- II 期和 III 期 EBC 患者的辅助治疗,包括 N0 的患者,获批范畴较以往 CDK4/6 抑制剂早期乳腺癌适用人群增加一倍有余。也期待瑞波西利可以早日在我国上市并纳入医保,惠及更多的患者。

邵志敏 教授
复旦大学附属肿瘤医院
● 复旦大学肿瘤、乳腺癌研究所长、大外科主任兼乳腺外科主任
● 中国抗癌协会乳腺癌专业委员会名誉主委
● 中华医学会肿瘤学分会副主任委员
● 上海市抗癌协会乳腺癌专业委员会名誉主任委员
● 上海市医学会肿瘤专科委员会主任委员
● 第八届亚洲乳腺癌协会主席
● St.Gallen乳腺癌大会专家团成员[1]Huppert LA, et.al. Systemic therapy for hormone receptor-positive/human epidermal growth factor receptor 2-negative early stage and metastatic breast cancer. CA Cancer J Clin. 2023;73(5):480-515.
[2]Rastogi P, et al. J Clin Oncol. 2024 Mar 20;42(9):987-993.[3]Slamon DJ,et al. Ther Adv Med Oncol. 2023 May 29;15:17588359231178125[4]Schäffler H, et al. Int J Mol Sci. 2023 Nov 15;24(22):16366. [5]Slamon D, et al. N Engl J Med. 2024 Mar 21;390(12):1080-1091.[6]Bardia A.et al. 2023 ESMO LBA23.[7]Denise Yardley, et al. 2024 ASCO. 512.[8]Fasching P, ET AL. 2024 ESMO LBA13