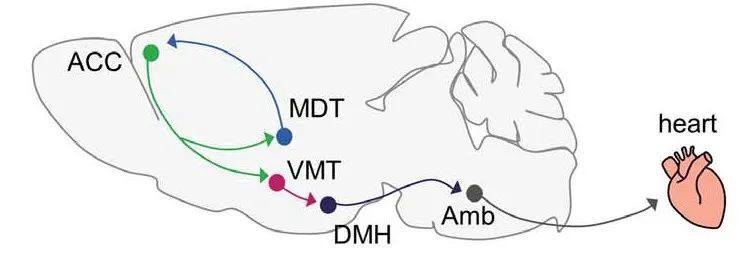
前扣带皮层(ACC)-腹内侧丘脑(VMT)-背内侧下丘脑(DMH)以及延髓腹部(Amb)-心脏通路
要点速览
1. 本研究建立了一个大鼠心率反馈系统,发现大鼠可以通过生物反馈强化学习来调节自己的心率。2. 大鼠在5天的训练后,心率可以降低约50%,并且这种降低心率的效果可以持续至少10天。3. 这种操作性心率降低是通过前扣带皮质(ACC)到腹内侧丘脑核(VMT)的神经通路调控实现的。4. ACC到VMT的theta节律刺激可以复制出操作性心率降低的效果。VMT神经元投射到背内侧下丘脑(DMH),DMH神经元又投射到核弓(Amb),Amb是通过迷走神经调控心脏的重要结构。5. 这一ACC-VMT-DMH-Amb的自上而下调控通路是操作性心率降低的神经机制。此外,这种持续的心率降低还可以引起焦虑相关行为的改变。背景
生理参数如心率(HR)、血压和体温主要由自主神经系统控制,但可以通过专门的训练并提供实时反馈来有意识地调节这些参数。 尽管这种生物反馈训练在临床应用方面有广泛潜力,但大脑-器官控制的神经机制仍然不太清楚。
受之前研究的启发,本研究建立了一个使用自由活动大鼠的心率反馈实验模型,旨在阐明心率反馈训练的神经机制及其相关的神经生理活动。研究发现,心率反馈训练可以引起大脑前扣带皮质(ACC)的theta节律活动,并激活连接ACC与丘脑腹内侧核(VMT)和内侧背侧核(MDT)的神经通路。这些神经通路最终通过连接下丘脑背内侧核(DMH)和延髓核缓慢性迷走神经核(Amb)的通路,调节心脏活动,从而实现对心率的自主调控。
结果
1. 闭环心率反馈刺激大脑可以使得大鼠实现操作性心率控制
本研究建立了一个使用自由活动大鼠的心率反馈实验模型,旨在阐明心率反馈训练的神经机制及其相关的神经生理活动。
实验设计如下:大鼠的心电图(ECG)被监测,每100毫秒计算一次平均心率。训练时,大鼠的目标心率设定为基线心率的15%以下。当大鼠的心率高于目标心率时,会刺激右侧感觉皮质;当心率低于目标心率时,会刺激左侧感觉皮质。当大鼠的心率降到目标心率以下时,会给予奖励性的内侧前脑束(MFB)刺激。这种训练持续3小时,连续进行5天。
结果显示,大鼠能在30分钟内开始降低心率,到第5天训练结束时,心率下降了约46%。这种心率下降持续至少10天,并伴有焦虑行为的减少和红细胞计数的增加。
- 使用一套电生理信号采集器采集心电图数据并使用API读取数据流。
- 每100 ms计算1秒窗口内的心率,基于心电图的RR间隔。数据经过滤波处理后,检测R波峰值确定心率。
- 通过向大脑皮质(barrel cortex或V1)施加1-5个刺激脉冲,反馈当前心率与目标心率的差异。刺激脉冲数量与心率偏差成正比。
- 每2秒进行一次评估,并通过API控制一个刺激器产生双相电流刺激皮质。
- 当大鼠将心率降至目标值以下10秒,则给予奖励性的内侧前脑束(MFB)刺激。
- 当大鼠获得10次奖励后,目标心率更新为前1分钟心率的15%降低,以促使大鼠持续降低心率。
2. 心率反馈训练可以导致大鼠出现持续性的系统性生理效应
大鼠在心率反馈训练过程中,其基线心率会逐渐降低,心率变异性也会增加,表明训练过程中存在慢性的副交感神经优势。训练结束后,大鼠的心率会持续低于训练前的基线水平,至少持续10天。这种持续性的低心率也伴有血压的降低。(后文称作“操控性低心率”)
此外,训练还会导致体温下降,最低可达29.7±1.8°C。但是,尽管出现了慢性低心率和低体温,大鼠的运动活动并没有减少。相反,训练后大鼠在开放场实验中表现出焦虑行为的减少,说明训练可能产生了抗焦虑的效果。
这种持续性的生理变化可能是由于一些代偿性机制的出现,如红细胞计数的增加。总之,心率反馈训练不仅能够短期调节心率,还可能产生一些长期的系统性生理效应。
图1. 闭环心率反馈刺激大脑可以使得大鼠实现操控性低心率。图1A和图1B显示,通过注射AAVdj-CAG-FLEX-GFP-2A-TetToxLc或AAVdj-CAG-FLEX-GFP到ACC并注射retroAAV2-pmSyn1-EBFP-Cre到VMT,可以抑制ACC到VMT的神经传递。这表明ACC到VMT的神经传递是操控性低心率所需的。图1C到图1F显示,通过注射AAV-CaMKIIa-ChR2-EYFP到ACC并在VMT植入光纤,可以通过7 Hz的蓝光刺激VMT诱导心率降低。而注射AAV-CaMKIIa-YFP到ACC并在VMT植入光纤,7 Hz蓝光刺激不会影响心率。这进一步证实了ACC到VMT的神经传递在操控性低心率中的作用。图1D到图1F显示,7 Hz蓝光刺激ACC到MDT通路也可以诱导心率降低,但ACC到AIC或M2通路刺激则不会影响心率。这表明ACC到VMT和ACC到MDT通路都参与了操控性低心率的调控。图1E和图1F显示,通过逆行性病毒示踪,发现ACC神经元是最主要的投射到DMH-投射VMT神经元的前突触神经元。而MDT和AIC则是主要的投射到VMT-投射ACC神经元的前突触神经元。这揭示了ACC-VMT-DMH-Amb通路是实现操控性低心率的自上而下的调控通路。图1I到图1J显示,DMH神经元确实投射到Amb,Amb则是通过迷走神经调控心脏的重要结构。这进一步证实了ACC-VMT-DMH-Amb通路在操控性低心率中的作用。LF/HF:是心率变异性(Heart Rate Variability, HRV)的一个指标,它反映了交感神经和副交感神经的平衡状态。具体来说,LF/HF是低频功率(Low Frequency, LF)与高频功率(High Frequency, HF)的比值。LF主要反映交感神经活动,HF主要反映副交感神经活动。LF/HF的升高表示交感神经活动增强,副交感神经活动相对减弱,即交感-副交感神经平衡偏向交感优势。相反,LF/HF的降低表示交感神经活动减弱,副交感神经活动相对增强,即交感-副交感神经平衡偏向副交感优势。高架十字迷宫(EPM)实验: EPM实验是一种常用于评估大鼠焦虑行为的实验方法。大鼠在EPM中会自然倾向于待在封闭的臂道,而不愿进入开放的臂道,因为开放臂会引起大鼠焦虑。训练可以减轻大鼠在EPM中的焦虑行为,表现为它们在开放臂上花费更多时间。旷场实验(OF): OF实验也是评估大鼠焦虑行为的一种方法。在OF中,大鼠倾向于远离中央区域,靠近墙壁。训练可以减轻大鼠在OF中的焦虑行为,表现为它们在中央区域上花费更多时间。明暗箱实验(LD): LD实验是另一种评估大鼠焦虑行为的方法。大鼠倾向于待在黑暗区域,而不愿进入明亮区域,因为明亮区域会引起大鼠焦虑
3. 心率反馈训练可以激活大鼠大脑皮层的前扣带皮质(ACC)和前岛皮质(AIC)区域
通过局部注射肌氨酸(muscimol)抑制ACC的神经活性,可以减弱心率反馈训练引起的缓慢心率 。而抑制AIC的神经活性则不会影响心率反馈训练的效果 。这表明ACC在操控性低心率中起重要作用,而AIC可能不参与这一过程。
进一步研究发现,在心率反馈训练过程中,ACC局部场电位(LFP)出现了明显的7.1 Hz的theta频段振荡,并且随着训练时间的增加,theta振荡的功率也逐渐增强 。同时,ACC神经元的放电也表现出与theta振荡相位锁定的特点 。这些结果表明,ACC的theta振荡可能参与了操作性缓慢心率的调控过程。
此外,示踪实验发现,ACC存在大量投射到丘脑腹内侧核(VMT)和内侧背侧核(MDT)的轴突纤维 。在心率反馈训练后,这些投射到VMT的ACC神经元表现出明显的c-Fos免疫反应。这进一步支持了ACC在实现操控性低心率中的重要作用。
图2. HR反馈诱导的心率降低需要前扣带皮质(ACC)神经元活动的参与。图2A和图2B显示,通过注射AAVdj-CAG-FLEX-GFP-2A-TetToxLc或AAVdj-CAG-FLEX-GFP到ACC并注射retroAAV2-pmSyn1-EBFP-Cre到VMT,可以抑制ACC到VMT的神经传递。这表明ACC到VMT的神经传递是操控性低心率所需的。图2C到图2F显示,通过注射AAV-CaMKIIa-ChR2-EYFP到ACC并在VMT植入光纤,可以通过7 Hz的蓝光刺激VMT诱导心率降低。而注射AAV-CaMKIIa-YFP到ACC并在VMT植入光纤,7 Hz蓝光刺激不会影响心率。这进一步证实了ACC到VMT的神经传递在操控性低心率的作用。图2D到图2F显示,7 Hz蓝光刺激ACC到MDT通路也可以诱导心率降低,但ACC到AIC或M2通路刺激则不会影响心率。这表明ACC到VMT和ACC到MDT通路都参与了操控性低心率的调控。图2E和图2F显示,通过逆行性病毒示踪,发现ACC神经元是最主要的投射到DMH-投射VMT神经元的前突触神经元。而MDT和AIC则是主要的投射到VMT-投射ACC神经元的前突触神经元。这揭示了ACC-VMT-DMH-Amb通路是操控性低心率的自上而下调控通路。图2I到图2J显示,DMH神经元确实投射到Amb,Amb则是通过迷走神经调控心脏的重要结构。这进一步证实了ACC-VMT-DMH-Amb通路在实现操控性低心率过程中的作用。此外,示踪实验发现,ACC存在大量投射到丘脑腹内侧核(VMT)和内侧背侧核(MDT)的轴突纤维 。在心率反馈训练后,这些投射到VMT的ACC神经元表现出明显的c-Fos免疫反应。这进一步支持了ACC在操控性低心率调控中的重要作用。图3. HR反馈诱导的心率下降需要从前扣带皮质(ACC)到腹内侧丘脑(VMT)的神经递质传递。图3A展示了病毒注射实验的设计。研究者将AAVdj-CAG-FLEX-GFP-2A-TetToxLc或AAVdj-CAG-FLEX-GFP病毒注射到前扣带皮质(ACC),同时将retroAAV2-pmSyn1-EBFP-Cre病毒注射到背内侧丘脑(VMT)。这种病毒注射方式可以选择性地表达TetToxLc或GFP蛋白于从ACC投射到VMT的神经元。图3B显示,当ACC神经元向VMT的神经传递被TetToxLc抑制时,心率反馈训练诱导的心率下降效果明显减弱。这表明ACC-VMT神经通路在操控性低心率中起关键作用。图3C展示了将ChR2基因导入ACC神经元的病毒注射实验设计。这种方法可以通过光刺激激活ACC神经元。图3D和3E显示,在脑片实验中,当用蓝光刺激ACC神经元的轴突终端时,VMT神经元会产生兴奋性突触后电流(EPSC)。这些EPSC可被谷氨酸受体拮抗剂DNQX和AP5所阻断,表明ACC到VMT的突触传递是谷氨酸能性的。图3F展示,当以7Hz的频率重复刺激ACC神经元时,EPSC幅度会逐渐增大,表现出短时程突触促进效应。这种7Hz频率的突触促进效应最为显著,暗示ACC-VMT神经通路可能在7Hz的节律中发挥作用。图4. 前扣带皮质(ACC)到背内侧丘脑(VMT)的神经通路参与调控大鼠的操控性低心率图4A显示,当使用光遗传学刺激前扣带皮质(ACC)投射到背内侧丘脑(VMT)的神经元时,大鼠会出现心率下降的现象。图4B进一步比较了不同刺激频率(0.5Hz、2Hz、7Hz、20Hz)对心率的影响,结果显示7Hz刺激具有最强的降心率效果。图4C表明,对于仅表达荧光蛋白的对照大鼠,7Hz光刺激不会引起心率下降。图4D显示,刺激从ACC投射到内侧丘脑(MDT)的神经元也可以引起心率下降,而刺激从ACC投射到前岛皮质(AIC)的神经元则不会产生这种效果。图4F表明,刺激ACC以外的次级运动皮层也不会引起心率下降。4. 大脑皮质前扣带区(ACC)通过多突触通路调控心脏
具体过程为 ACC神经元投射到丘脑腹内侧核(VMT),VMT神经元又投射到下丘脑背内侧核(DMH),DMH神经元最终投射到核团旁核(Amb)并支配心脏的副交感神经。这一通路的激活可以诱发大脑对心率的自主调控,使大鼠能够通过生物反馈训练主动降低心率。此外,这一通路的激活还可以引起焦虑相关行为的改变,表明大脑对心脏的调控与情绪状态密切相关。图 5. ACC→VMT→DMH→Amb通路构成了操控性低心率的自上而下调控通路图5A-5D显示,通过在背内侧丘脑(VMT)注射病毒载体表达光敏蛋白ChR2,可以在急性脑片实验中观察到VMT神经元对蓝光刺激产生兴奋性突触电流(EPSC)。这种兴奋性传递在7Hz刺激时表现出短期增强。图5E-5F使用逆向单突触病毒示踪技术发现,投射到背内侧下丘脑(DMH)的VMT神经元主要来自ACC,而ACC神经元主要来自内侧丘脑(MDT)和前岛皮质(AIC)。图5G-5H进一步证实,投射到VMT的ACC神经元主要接受来自MDT和AIC的突触输入。图5I-5J显示,DMH神经元可以通过轴突投射到迷走神经核(Amb),而Amb神经元则可以通过迷走神经调控心脏。图5K总结了这条从ACC到心脏的多突触神经通路(ACC→VMT→DMH→Amb),这可能是调控心率的重要"自上而下"机制总结
本研究建立了一个大鼠心率(HR)生物反馈系统,证明大鼠可以通过基于生物反馈的强化学习来调节自己的心率。心率的降低是由中枢多巴胺信号介导的,但不是主要由呼吸调节或麻醉下引起的。因此,这种操控性低心率很可能是由自主的自上而下机制产生的。
研究发现,生物反馈诱导的缓慢心率伴有前扣带皮质(ACC)的theta节律活动。因为由物理刺激(如浸水、缺氧和超声波)引起的反射性缓慢心率即使在麻醉或去脑动物中也会发生,并且不需要ACC,所以ACC可能作为心率调节的自上而下中心。这一想法可能与人类冥想过程中ACC theta振荡增加有关。
来自ACC的光纤记录显示,训练过程中theta振荡并非完全缺失,但很微弱;而投射到VMT的ACC神经元则表现出强烈的theta振荡。这表明,ACC的一个细胞亚群(即投射到VMT的神经元)被招募参与theta振荡。ACC可能由多个并行回路组成,能同时处理不同层次的信息,这与ACC参与疼痛、认知、注意和情绪等多种功能的事实一致。
ACC参与自主神经系统的调节,电刺激ACC可引起自主反应。事实上,ACC神经元投射到下丘脑和脑干等主要自主结构。然而,从ACC到心脏的详细神经通路仍有待阐明。本研究采用单突触和双突触示踪技术,揭示了从ACC到心脏的整个神经通路。研究还发现,投射到VMT和MDT的ACC神经元在训练过程中都被激活。我们推测,ACC和MDT形成一个相互回路,作为theta振荡的发生器。然后,这一回路的活动从ACC传递到VMT,随后传递到DMH、Amb和心脏。本研究为心脑相互作用的研究开辟了新的途径。
全澜闭环调控解决方案
全澜的闭环调控解决方案能够高效地实现本研究中的闭环心率反馈刺激。该方案由AR4M多模态无线电生理遥测系统、C64闭环刺激器和闭环调控软件平台(APIs)组成,可实时、长时程监测多模态电生理信号(包括EEG、ECG、LFP、EMG),并提供高精度的颅内电流刺激。通过这一系统,研究中的闭环调控方案可在一套设备中全面实现。全系统软硬件均为自研,具备极高的扩展性和全面的支持,欢迎试用。